ORIJINMD est le Programme de soutien aux patients qui prennent JINARC.
Notre engagement inébranlable envers vous et vos patients se poursuit.

PrJINARCMD est le premier traitement indiqué dans la MPRAD1*.
Vous pouvez compter sur notre expérience de plus de 10 ans au Canada†.
* La pertinence clinique comparative est inconnue.
† La pertinence clinique est inconnue.
Services du Programme ORIJIN qui vous sont offerts, à vous et à vos patients

Aucun coût additionnel pour la marque JINARC
Les patients bénéficiant d’une assurance privée ont accès à une carte d’aide au paiement en pharmacie. Celle-ci vise à aider les patients en éliminant les coûts déboursés de leur poche pour la marque JINARC. Le Programme couvre toute différence de coût entre JINARC et le régime privé d’assurance du patient.

Services infirmiers spécialisés
Nos infirmier(ère)s expert(e)s offrent des soins personnalisés, de l’éducation sur le traitement et un soutien émotionnel pour aider vos patients tout au long de leur parcours avec la maladie polykystique rénale.
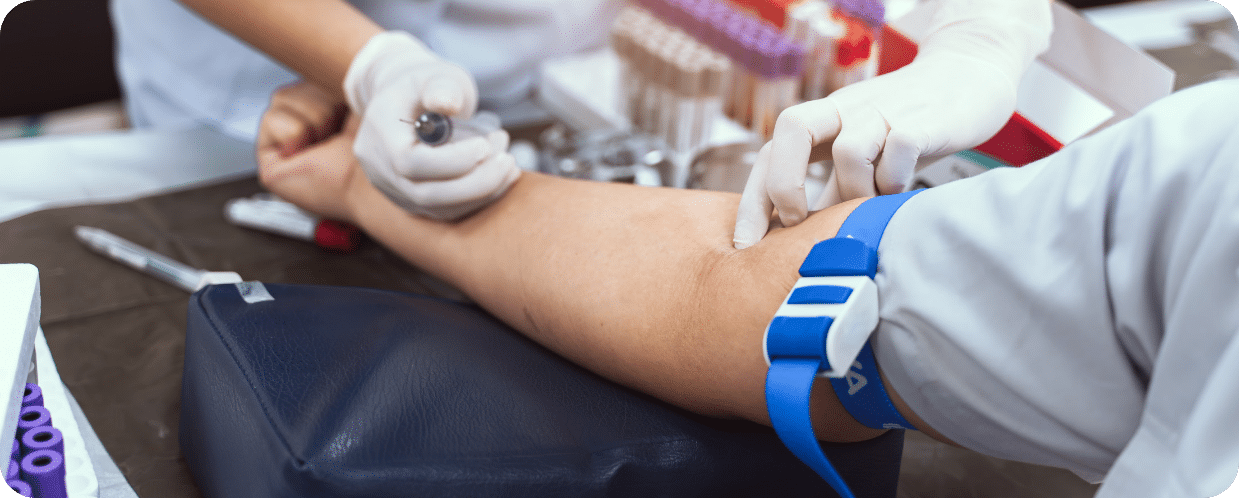
Programme pratique d’analyses sanguines à domicile
Nous offrons un programme pratique d’analyses sanguines à domicile ou de rappels téléphoniques pour la surveillance de la fonction hépatique, afin d’assurer un accès facile et des résultats en temps opportun.

Services de pharmacie et de livraison
Les patients ont accès à une équipe de pharmacie expérimentée dans le traitement par JINARC et à un service de livraison flexible du médicament à l’endroit de leur choix, que ce soit à la maison ou au travail.

Soutien nutritionnel et webinaires éducatifs
Nous offrons des webinaires éducatifs animés par des diététistes spécialisés dans la MPRAD, afin d’aider les patients à faire des choix éclairés en matière d’alimentation et de mode de vie qui leur permettront d’optimiser leur traitement par JINARC.

Surveillance de la fonction hépatique
Le Programme contrôlé de distribution et de surveillance de l’innocuité hépatique (DSIH) de JINARC, géré par le Programme ORIJIN, valide les inscriptions, assure l’expédition de JINARC à la bonne pharmacie, envoie des rappels d’analyses sanguines aux patients, et effectue le suivi des résultats des tests de fonction hépatique.
83,6 % des patients traités par JINARC ont poursuivi leur traitement pendant la première année suivant son instauration. Les taux de rétention ont été déterminés en fonction d’une période de 36 mois, jusqu’en juillet 202533.
PrJINARCMD (tolvaptan) est indiqué pour ralentir la progression de l’hypertrophie des reins et le déclin de la fonction rénale chez les patients adultes atteints de la maladie polykystique rénale autosomique dominante (MPRAD). Dans la MPRAD, l’hypertrophie reflète la charge kystique des reins2.
Le fabricant de JINARC a mis en œuvre un programme de surveillance de l’innocuité régissant l’utilisation de JINARC et l’accès au produit : le Programme de distribution et de surveillance de l’innocuité hépatique de JINARC. Au Canada, tous les prescripteurs et les patients doivent être inscrits à ce programme afin de prescrire ou de recevoir JINARC.
Cliquez ici ou consultez la monographie de JINARC au jinarcmonographie.ca pour obtenir des renseignements importants sur :
- les contre-indications : recommandation d’abandon définitif de l’usage du tolvaptan dans le passé; hypersensibilité connue ou présumée au tolvaptan, à la benzazépine ou aux dérivés de la benzazépine (p. ex., mirtazapine), ou à l’un des excipients du produit; hypovolémie; hypernatrémie; anurie; absence d’accès à des liquides ou incapacité du patient à répondre à la sensation physiologique de soif; antécédents ou présence de signes ou de symptômes d’une atteinte ou d’une lésion hépatique importante, à l’exception d’une maladie polykystique hépatique non compliquée; usage concomitant d’inhibiteurs puissants du CYP3A; grossesse ou allaitement; présence de l’un des rares troubles héréditaires suivants : intolérance au galactose, déficit en lactase de Lapp ou malabsorption du glucose et du galactose;
- les mises en garde et précautions les plus importantes sur la toxicité hépatique idiosyncrasique;
- d’autres mises en garde pertinentes sur la déshydratation, les interactions médicament-médicament, l’hépatotoxicité, l’hypernatrémie, l’hyperkaliémie, l’hyperuricémie, l’hypotension, les anomalies du taux sérique de sodium, les analogues de la vasopressine et la conduite automobile ou l’utilisation de machineries;
- les conditions d’utilisation clinique, les effets indésirables, les interactions, la posologie et la surveillance.
La monographie est également offerte sur demande, en appelant au 1 877 341-9245.
Renseignements importants sur l’innocuité de PrJINARCMD
Indications et usage clinique
PrJINARCMD (tolvaptan) est indiqué pour ralentir la progression de l’hypertrophie des reins et le déclin de la fonction rénale chez les patients adultes atteints de la maladie polykystique rénale autosomique dominante (MPRAD). Dans la MPRAD, l’hypertrophie reflète la charge kystique des reins.
- Dans le but de sélectionner les patients les plus susceptibles de bénéficier des effets de JINARC, des essais cliniques ont été menés auprès de patients atteints de MPRAD ayant un volume rénal total (VRT) ≥ 750 mL et/ou une fonction rénale correspondant à un débit de filtration glomérulaire estimé par la formule CKD-EPI ≥ 25 mL/min/1,73 m2, au moment de l’instauration du traitement.
- Le traitement par JINARC doit être amorcé et suivi sous la supervision d’un néphrologue ou d’un médecin spécialiste possédant une expertise dans la prise en charge de la MPRAD et ayant une excellente compréhension des bienfaits et des risques associés au traitement par le tolvaptan, notamment en ce qui concerne l’hépatotoxicité et les mesures de surveillance requises.
- La décision d’amorcer un traitement par JINARC doit être mûrement réfléchie et faire l’objet d’une discussion préalable entre le prescripteur et le patient, au sujet des bienfaits et des risques éventuels du traitement. Lors d’un commun accord pour entreprendre le traitement par JINARC, le formulaire d’entente entre le patient et le prescripteur (FEPP) spécifique au produit et au fabricant devra être signé et dûment documenté énonçant les critères pertinents de sélection du patient à considérer, les bienfaits et les risques attendus du traitement et l’obligation de surveiller la fonction hépatique.
- Programme contrôlé de distribution et de surveillance de l’innocuité hépatique de JINARC : JINARC (tolvaptan) est utilisé dans le traitement des patients atteints de MPRAD et est offert uniquement par l’intermédiaire d’un programme contrôlé de distribution et de surveillance de l’innocuité hépatique (DSIH) spécifique au produit et au fabricant mis en œuvre et maintenu par, ou pour, le détenteur d’une autorisation de mise en marché de JINARC. L’obtention d’un FEPP spécifique au produit et au fabricant dûment signé est nécessaire pour inscrire un patient au Programme DSIH. Pour obtenir de plus amples renseignements sur le programme, veuillez téléphoner au 1 844 254-6272.
- L’innocuité et l’efficacité de JINARC chez les patients âgés n’ont pas été établies (> 65 ans).
Contre-indications
JINARC est contre-indiqué dans les cas suivants :
- recommandation d’arrêt définitif de l’usage du tolvaptan dans le passé;
- hypersensibilité connue ou présumée au tolvaptan, à la benzazépine ou aux dérivés de la benzazépine (p. ex., mirtazapine), ou à l’un des excipients du produit;
- hypovolémie;
- hypernatrémie;
- anurie;
- absence d’accès à des liquides ou incapacité du patient à répondre à la sensation physiologique de soif;
- antécédents ou présence de signes ou de symptômes d’une atteinte ou d’une lésion hépatique, à l’exception d’une maladie polykystique hépatique non compliquée;
- usage concomitant d’inhibiteurs puissants du CYP3A, p. ex., kétoconazole, itraconazole, clarithromycine, télithromycine, ritonavir, indinavir, nelfinavir, saquinavir, néfazodone;
- grossesse;
- allaitement;
- présence de l’un des rares troubles héréditaires suivants : intolérance au galactose, déficit en lactase de Lapp ou malabsorption du glucose et du galactose.
Autres mises en garde et précautions pertinentes
- Déshydratation
- Interactions avec des inhibiteurs modérés du CYP3A, des inducteurs du CYP3A et des inhibiteurs de la glycoprotéine P
- Hépatotoxicité : insuffisance hépatique aiguë
- Anaphylaxie
- Hypernatrémie : L’utilisation concomitante de JINARC et de solutions salines hypertoniques ou de médicaments pouvant faire augmenter les concentrations sériques de sodium doit être évitée.
- Hyperkaliémie
- Hyperuricémie
- Hypotension : La prise concomitante d’antihypertenseurs peut entraîner une fréquence accrue d’événements indésirables liés à l’hypotension, notamment les étourdissements et la syncope.
- Les anomalies du taux sérique de sodium doivent être corrigées avant l’instauration du traitement par JINARC.
- Les femmes aptes à procréer doivent suivre une méthode contraceptive efficace.
- Analogues de la vasopressine : L’administration concomitante avec JINARC n’est pas recommandée.
- Le patient qui conduit un véhicule ou fait fonctionner des machines pendant le traitement par JINARC doit faire preuve de prudence.
Pour de plus amples renseignements
Consulter la monographie de produit à l’adresse jinarcmonographie.ca pour connaître les effets indésirables, les interactions, la posologie, les épreuves de surveillance et les conditions d’utilisation clinique de ce produit. La monographie est également offerte sur demande, en appelant au 1 877 341-9245.
